Додаток № 2
Використання дидактичних ігор.
Гра «Хімічне печиво»:
Тема: «Солі» (8 клас)
Учням пропонується у порожні комірки таблиць записати формули відповідних солей.
| Метал | |||
| Кислота | Na | Zn | Al |
| HNO3 | |||
| H2SO3 | |||
| H3PO4 | |||
| Метал | |||
| Кислота | Ag | Mg | Fe(ІІІ) |
| HPO3 | |||
| H2S | |||
| H2CO3 | |||
Гра «Третій зайвий»:
Тема: «Основні класи неорганічних сполук» (8 клас)
Вибрати з кожного ряду зайву речовину.
| BaS | CO2 | CaO |
| HNO3 | H2O | HCl |
| Na2SO4 | H3PO4 | BaCl2 |
| Ca(OH)2 | NaOH | Al(NO3)3 |
| P2O5 | MgCl2 | SO2 |
Гра «Хрестики-нулики».
Тема: Узагальнення знань з теми «Основні класи неорганічних сполук»
(8 клас)
Знайдіть правильну відповідь:
а). Одновалентні кислотні залишки
| NO3 | S | CO3 |
| PO4 | J | SO3 |
| SO4 | SiO3 | Br |
б). Формули солей
| P2O5 | NaOH | ZnSO4 |
| HNO3 | CaO | BaCl2 |
| CO2 | H2S | K2S |
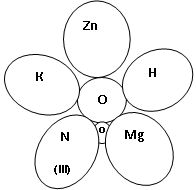
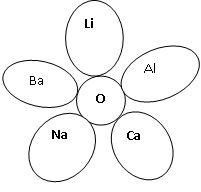
Гра «Квітка-семицвітка».
Тема: «Оксиди» (8 клас)
Скласти формули оксидів та дати назву оксидам.
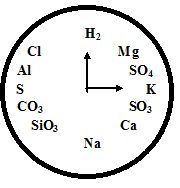
Гра «Хімічний годинник»
Тема: «Кислоти» (8 клас)
За допомогою «Хімічного годинника» скласти хімічні формули кислот.
Гра «Хто більше?»
Тема: Узагальнення знань з теми «Основні класи неорганічних сполук»
(8 клас)
На швидкість скласти найбільшу кількість сполук.
1). Скласти формули п’яти кислот, використовуючи такі хімічні символи:
|
|
|
H2 |
NO3 |
|
|
|
|
Cl |
H3 |
SiO3 |
PO4 |
|
|
H |
SO4 |
CO3 |
J |
S |
H |
2). Скласти формули п’яти солей, використовуючи такі складові частини:
|
|
|
K2 |
Ba |
|
|
|
|
Cl2 |
Na2 |
SO4 |
Cu |
|
|
Zn |
SO3 |
S |
CO3 |
NO3 |
Mg |
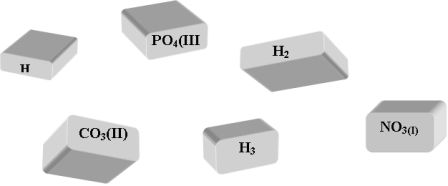
Гра «Пасьянс»
Тема: «Кислоти, їх склад, назви та класифікація».
На столи учнів даються картки, необхідно скласти формули кислот.
Напркилад:
Розгадування кросвордів (9 клас)
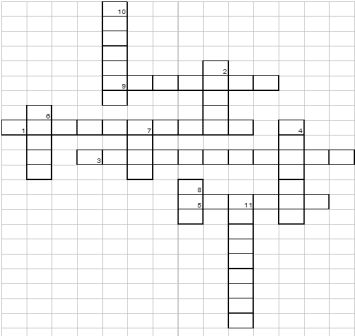
«Насичені вуглеводні».
- Сполуки, молекули яких складаються з атомів Карбону і Гідрогену.
- Найпростіший представник алканів.
- Прізвище вченого, який виділив циклоалкани з бакинської нафти.
- Вуглеводні з замкнутими карбоновими ланцюгами.
- Назва насичених вуглеводнів за функціональною номенклатурою.
- Четвертий представник гомологічного ряду насичених вуглеводнів.
- Прізвище вченого, який досліджував хімічні властивості насичених вуглеводнів.
- Агрегатний стан характерний для перших чотирьох представників алканів за нормальних умов.
- Альтернативна назва циклоалканів.
- Гомологічний розрив зв’язків карбонового ланцюга, який протікає за нагрівання в присутності каталізатора.
- Вчений, який досліджував нітрування алканів.
Гра «Розсипанка»
Тема: «Основні класи неорганічних речовин» (8 клас)
Робота може бути як в парах, так і індивідуально на швидкість.
Одного разу, якось Незнайко потрапив один до хімічного кабінету і вирішив його добре роздивитися. Побачивши реактиви, почав їх знімати з поличок з написами: «Оксиди», «Основи», «Кислоти», «Солі». Всі скляночки з речовинами акуратно склав на столі довільно. Після того, як роздивився, то злякався, а якже їх правильно скласти на поличкі. Допоможіть розгубленому Незнайкові розкласти все по місцях. Незабудьте дати назви речовинам!
Учні отримують на аркуші перелік формул речовин: Al(OH)3, FeO, NaCl, H2O, HCl, Mg, Ca(OH)2, Cu(OH)2, NaNO3, KI, LiOH, H3PO4, CaO, H2SO4, ZnS, CO2, NaF, CaCO3, Ba(OH)2, H2 SiO3.
Із даного переліку потрібно виписати окремо формули оксидів, основ, кислот, солей.
Конкурс «Математичний»
Тема: «Періодичний закон і періодична система» (7,8 клас)
За даними формулами знайти хімічний елемент.
- (а-b)2 = c
a – кількість нейтронів в атомі Кальцію;
b – протонне число атома Фосфору;
c – порядковий номер елемента
Відповідь: Манган
- a2 + 2ab+b2 = e
a – протонне число атома Гідрогену
b – загальна кількість електронів в атомі Карбону
e – порядковий номер елемента
Відповідь: Індій
Вправа «Відгадай елемент»
Тема: «Періодичний закон і періодична система» (7,8,10 клас)
- Порядковий номер елемента 17
- Заряд ядра атома + 22
- Відносна атомна маса елемента 64
- Загальна кількість електронів у атомі 15
- У ядрі цього атома 21 протон
- Елемент 2 періоду V групи
- Радіоактивний елемент 7 періоду ІІ групи головної підгрупи
- Сума протонів та нейтронів у атомі цього елемента дорівнює 24
- Хімічний елемент входить до складу сульфатної кислоти мешкає в 3 періоді VІ групи
- Елемент, що відповідає за міцність кісток людини. Його відносна атомна маса 40
- Нуклонне число в атомі елемента 65
- Хімічний елемент 4 періоду VІІІ групи побічної підгрупи, що входить до складу крові людини
Вправа «Впізнай речовину»
Завдання: У пробірках під номерами 1,2,3,4 знаходяться розчини H2SO4, KOH, Ba(NO3)2, Na2CO3.
а) Як поетапно визначити ці розчини? Запропонуйте свій план і реалізуйте його з допомогою реактивів, що є в лотках, дотримуючись правил техніки безпеки.
б) У результаті взаємодії в яких попарно взятих речовин задовольняються три умови протікання реакці йонного обміну до кінця? А саме – утворення осаду.
Використання інтерактивних методів на уроках хімії у 8 класі.
На комбінованому уроці «Періодична система хімічних елементів Д.І.Менделєєва» учні виконують інтерактивні завдання.
Виконання завдань
Завдання 1. Вірю – не вірю
Із запропонованих тверджень виберіть правильні.
- Хімія – це наука, яка вивчає хімічні речовини.
- Усі хімічні речовини можуть перебувати у складі чистої речовини чи суміші.
- Суміш є однорідною, якщо компоненти суміші можна побачити неозброєним оком.
- Прикладами однорідних сумішей є повітря, молоко, газована вода та суміш олії з водою.
- До неоднорідних сумішей можна віднести кров, грунт, дощову воду, суміш піску з водою.
- Речовина складається з молекул, молекули – з атомів.
- Атоми складаються з ядра та позитивно зарядженої електронної оболонки.
- До складу ядра входять протони та нейтрони.
- Протон має позитивний заряд.
- Атом у цілому електронейтральний.
- Йони, на відміну від атомів, мають позитивний або негативний заряд.
- Найбільш поширеним елементом у Всесвіті є Карбон.
Завдання 2. Виправ помилки
Учням пропонуються речення з помилками. Помилки треба знайти та виправити.
- Речовина складається з молекул, а ті, у свою чергу, - з протонів (Атомів).
- Атом складається з протонів та електронної оболонки (ядра).
- Ядро має негативний заряд, електронна оболонка – позитивний (навпаки).
- Маса нейтрона дорівнює одиниці, заряд – позитивний (відсутній).
- Маса протона також дорівнює одиниці, а заряд – відсутній (заряд негативний, маса відсутня).
- Найбільш поширеним елементом у Всесвіті є Гелій (Гідроген).
- Йони мають негативний заряд (позитивний).
- Найбільш поширеним елементом на Землі є Гідроген (Оксиген).
- Однакові за будовою протони, з’єднуючись між собою утворюють хімічний елемент (Атоми).
- Заряд ядра атома обумовлюють електрони (Протони).
Завдання 3. Третій зайвий
- Сульфур, Нітроген, Кисень (Кисень – речовина, Сульфур та Нітроген – хімічні елементи).
- Протони, нейтрони, Гідроген (протони, нейтрони – нуклони ядра, а Гідроген - хімічний елемент).
- Золото, молоко, повітря (повітря, молоко – суміші, а золото – речовина).
- Олія з водою, повітря, бульйон (олія з водою, бульйон – неоднорідні суміші, повітря – однорідна суміш).
Завдання 4. Усний диктант
Учитель вказує назву хімічного елемента, а учні піднімають картку з його символом: Берилій, Оксиген, Флуор, Кальцій, Магній, Фосфор, Аргон, Бор, Калій, Алюміній.
Мотивація навчальної діяльності
- Чи любите ви писати листи? Мабуть так. А що ви вказуєте на конверті? (Прізвище, ім’я, адресу). А навіщо? (Щоб лист дійшов до адресата). Отже, кожна людина має своє прізвище, ім’я, адресу: місто, вулицю, будинок, квартиру.
- Чи мають адресу хімічні елементи? Де їх можна знайти, якщо в цьому є потреба? На ці питання ми повинні знайти відповідь сьогодні на уроці.
Оголошення теми та мети уроку…
Використання інтерактивних методів на уроках хімії у 9 класі
Частина уроку «Узагальнення знань з теми «Електролітична дисоціація. Реакції йонного обміну між розчинами електролітів». (проводиться із застосуванням технології інтерактивних методів).
- Зупинка «Діалогічна»
Завдання
Повторити терміни, працюючи в парі «Вчитель – учень». Група, яка швидше закінчить діалог, отримає додатковий бал.
- Зупинка «Мозковий штурм»
Завдання 1.
а) підготувати одне запитання до іншої групи і поставити його (запитання і відповідь оцінюються одним балом);
б) представники груп працюють біля дошки, а група на місці
Завдання 2.
Користуючись таблицею «Розчинність кислот, основ і солей у воді», визначте, у результаті взаємодії яких розчинів реакції обміну відбуваються до кінця. Чому? Складіть рівняння в молекулярній, повній та скороченій йонній формах.
- Зупинка «Третій зайвий» (2 бали)
Завдання
З кожних трьох йонів викресліть той, що не взаємодіє з двома іншими з утворенням осаду, газу чи води. Між двома іншими, що залишилися, складіть йонні рівняння (скорочені й повні) та на їх основі – молекулярні.
К+ , Al3+ ,
- Зупинка «Роздумів»
Завдання
З курсу біології відомо, що до складу шлункового соку входить хлоридна кислота. Для зниження кислотності в шлунку застосовують питну соду NaHCO3. Чому питна сода знижує кислотність шлункового соку.