Тема: Хімічні властивості алкенів і алкінів
Мета: познайомити учнів з хімічними властивостями алкенів і алкінів на прикладі етилену і ацетилену: реакції окиснення і приєднання. Формувати навички й уміння складати рівняння хімічних реакцій.
Обладнання : мультимедійна презентація уроку.
Тип уроку: комбінований
Хід уроку.
І. Актуалізація опорних знань.
Бесіда
1. Які гомологічні ряди вуглеводнів ви знаєте?
2. Напишіть загальні формули кожного з рядів.
Перевірка домашнього завдання:
№12 ст. 149
№ 13 ст. 149
Кросворд
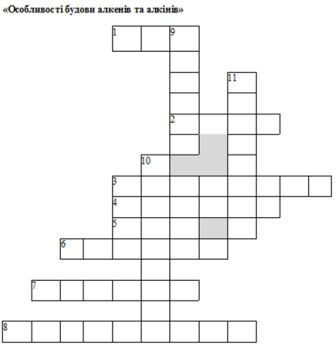
По горизонталі:
1. Кількість гібридних хмар в атомі С в молекулі ацетилену
2. Міжнародна назва алкену, що містить два атома С.
3. Як можна назвати одним словом наступні речовини: етен, пропен, бутен, пентен.
4. Перший представник гомологічного ряду алкенів.
5. Кількість гібридних хмар в атомі С в молекулі етилену
6. Ненасичені вуглеводні, в молекулах яких між атомами С є 1 потрійний зв'язок.
7. Ненасичені вуглеводні, в молекулах яких між атомами С є 1 подвійний зв'язок.
8. Який зв'язок обов'язковоо є в алкенах
По вертикалі:
9. Як можна назвати речовину СН2 = СН – СН2 – СН3
по відношенню до речовини до речовини СН2 = С– СН3
СН3
10. Який зв’язок обов’язково є в молекулах алкінів
11. Перший представник гомологічного ряду алкінів.
ІІ. Мотивація навчальної діяльності
Властивості речовин визначаються будовою речовини. Пригадайте алкани (насичені в.в.). Який зв’язок між атомами С в молекулах алканів? (простий) Це були не дуже активні речовини.
Який зв’язок між атомами С у алкенів і алкінів? (подвійний і потрійний).
Мета уроку: з’ясувати як поява кратних зв’язків в будові речовини відображається на її хімічних властивостях? В які реакції вступають етилен та ацетилен, а також їх гомологи. Що при цьому утворюється? Навчитися писати найпростіші рівняння реакцій.
ІІІ. Вивчення нового матеріалу.
Хімічні властивості алкенів та алкінів.
І. Реакції окиснення
1) Горіння або повне окиснення
С2Н4 + 3О2 → 2СО2 + 2Н2О +Q світне полум’я
2С2Н2 + 5О2 → 4СО2 + 2Н2О +Q кіптяве полум’я
Проблемне питання:Чому етан горить майже безбарвним полум’ям, алкени – світнім, а алкіни – кіптявим?
Чим більша масова частка Карбону, тим більш кіптявим буде полум’я. У етану масова частка Карбону найменша – Карбон швидко згорає (етан горить безбарвним полум’ям). У етану масова частка Карбону більша, тому перед тим як згоріти Карбон розжарюється (ми бачимо світне полум’я). У ацетилена масова частка Карбону найбільша, тому Карбон не весь згорає із-за нестачі кисню (ми бачимо кіптяве полум’я).
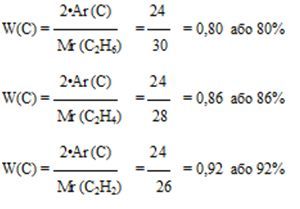
2) Часткове окиснення
КMnO4
С2Н4 + Н2О + О → CH2 – CH2
| |
OH OH
Якісна реакція на кратний зв’язок. Фіолетовий колір калій перманганату знебарвлюється.
ІІ. Реакції приєднання
1) Приєднання водню ( гідрування, гідрогенізація)
К
СН2 = СН2 + Н2 → СН3 – СН3
етен етан
К
СН ≡ СН + Н2 → СН2 = СН2
ацетилен етен
К
СН ≡ СН + 2 Н2 → СН3 – СН3
ацетилен етан
2) Приєднання галогенів (галогенування)
СН2 = СН2 + Br2 → СН2Br – СН2Br
СН ≡ СН + Br2 → СН2 Br = СН2 Br
СН ≡ СН + 2Br2→ СНBr2 – СНBr2
Якісна реакція на кратний зв’язок. Бурий колір брому знебарвлюється.
3) Приєднання галогеноводнів (гідрогалогенування, гідроген галогенування)
СН2 = СН2 + НBr → СН3 – СН2Br
СН ≡ СН + НBr → СН2 = СНBr
4) Приєднання води (гідратація)
СН2 = СН2 + Н2О → СН3 – СН2ОН
Добування етилену і ацетилену.
- Дегідрування алканів (відщеплення водню)
к
С2Н6 → С2Н4 + Н2
к
С2Н6 → С2Н2 + 2Н2
- Етилен добувають нагріванням етилового спирту з Н2SO4 конц - дегідратація
Н2SO4
С2Н5ОН → С2Н4 + Н2O
t
- Ацетилен добувають з кальцій карбіду мал. 89 ст 145 Н.М. Буринська, 9 кл
СаСО3 → СаО + СО2
СаО + 3С → СаС2 + СО
СаС2 + 2Н2О → С2Н2 + Са(ОН)2
- Ацетилен добувають термічним розкладом метану.
1500°С
2СН4 → С2Н2 + 3Н2
Закріплення набутих знань
(Фронтальна бесіда, виконання вправ і задач )
1.Порівняйте хімічну активність насичених вуглеводнів (алканів) і ненасичених вуглеводнів (алкенів і алкінів).
2. Здійснити перетворення:
CО2 С2Н4Cl2
↑ ↑
С → СН4 → С2Н2 → С2Н4 → С2Н6 →СО2
↓ ↓
С2Н2Br4 С2Н5Cl
3. Вам дано дві речовини. Одна з них етан, а інша – етилен. Запропонуйте, як можна розпізнати ці речовини.
4. Вкажіть, яку масу хлору може приєднати етен кількістю речовини 0,1 моль.
5.Визначте невідомий вуглеводень у реакції
2СхНу + 11О2 → 8СО2 + 6Н2О
Домашнє завдання:
§22 Н.М. Буринська, 9 кл
Впр. 9 ст 149